
一、引言:抗体药物的ADCC效应
随着生物技术的迅速发展,抗体药物已成为生物制药领域中最受关注的热点之一。抗体依赖细胞介导的细胞毒作用(antibody-dependent cell-mediated cytotoxicity, ADCC),是抗体发挥作用进而抵御疾病的重要作用方式。当抗体的Fab段特异性结合病毒感染的细胞或肿瘤细胞的抗原表位后,其Fc区可与杀伤细胞(NK细胞,巨噬细胞)上的活化受体Fcγ受体结合,从而激活效应细胞,释放细胞毒物质裂解并杀伤肿瘤细胞。
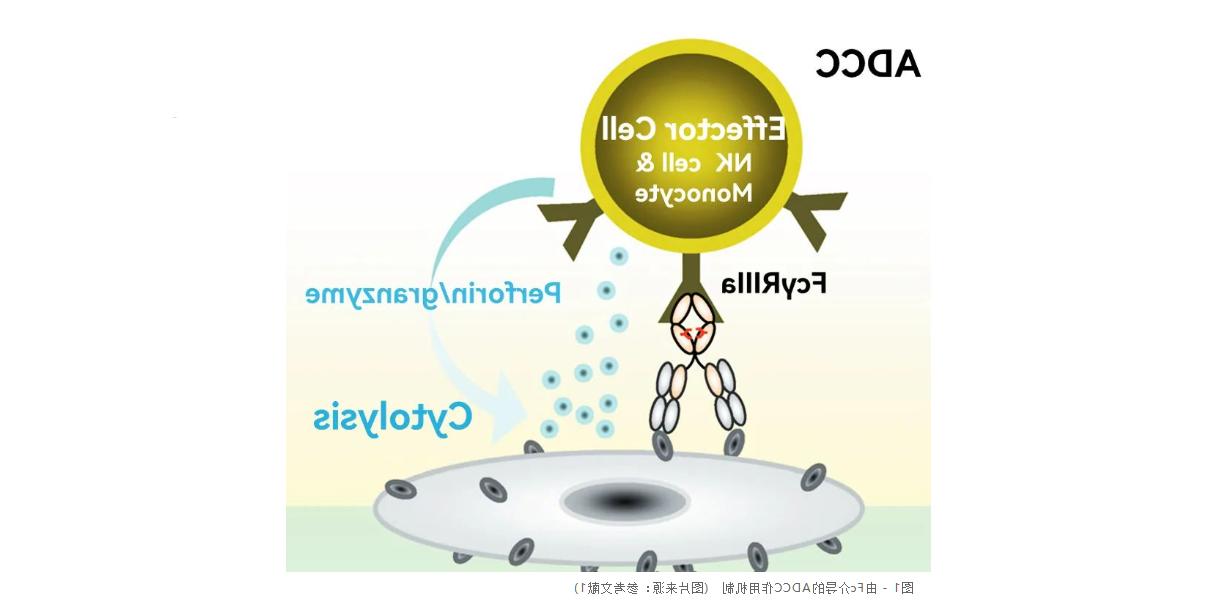
大量临床研究证明ADCC作用是抗体发挥效果的主要方式之一,如Rituximab, Obinutuzumab, Trastuzumab和Alemtuzumab。抗体介导的ADCC强弱与其对Fc受体的亲和力高低正相关。对抗体Fc段的糖基化改造可以提高ADCC活性,推荐全球十大博彩公司排行榜拥有自主平台的ADCC增强特色细胞株(CHOK1-AF),通过去除岩藻糖(Fucose)糖基化从而大幅增强抗体的ADCC活性,该宿主细胞已在多个临床I/II/III抗体项目中显示出良好的适用性、安全性和优异的临床表现。
延伸阅读:
二、ADCC细胞生物学活性检测要素
抗体药物的生物学活性评估,包括体外药效和产品放行,除Fcγ受体的亲和力/结合活性以外,还需要进行ADCC细胞生物学活性检测。ADCC细胞生物学活性检测,其整个过程有三个重要条件:抗体药物、靶细胞以及效应细胞。因此,在进行ADCC细胞生物学活性检测时,除根据ADCC效应选择合适的效应细胞外,还需要筛选出细胞表面高表达目标抗体可识别的靶细胞,从而确定合适的检测方法。

2.1. 效应细胞选择
PBMC(外周血单核细胞):PBMC作为效应细胞,可以反映最真实的杀伤效果,且该系统最接近体内免疫微环境。但原代PBMC细胞获取的成本相对较高,操作复杂,且批间一致性较差。
NK-92MI-CD16a工程细胞系:采用细胞膜上稳定表达CD16a(FcγRIIIa)的NK-92MI细胞作为效应细胞,抗体与效应细胞表面受体结合后,激发效应细胞的杀伤活性,直接杀伤靶细胞。NK-92MI-CD16a作为连续传代的工程细胞系,试验成功率高且可重复性好,除可进行体外药效检测,还适合作为放行检测方法的效应细胞。
2.2. 靶细胞选择
以野生型肿瘤细胞系作为靶细胞:人源的野生型癌细胞具有病理代表性,但肿瘤细胞系表面复杂性会导致较大的失败风险,需要花费较长的时间筛选合适的靶细胞。
以过表达靶点的细胞系作为靶细胞:构建成功的过表达靶点的工程细胞系的靶点表达量高,作为靶细胞时ADCC杀伤效果较好,但构建细胞系会产生额外成本,周期较长。
2.3. 检测方法
细胞毒性测试(Cytotoxicity assay):靶细胞被裂解后,细胞质中的乳酸脱氢酶(LDH)会释放到培养基上清中,上清中LDH的释放量与靶细胞裂解呈正相关,通过对上清液中的乳酸脱氢酶(LDH)进行定量,可检测靶细胞被杀伤的程度。

三、经典案例
推荐全球十大博彩公司排行榜的ADCC细胞生物学活性检测技术平台可针对不同的ADCC生物学活性实验需求为客户提供定制化的ADCC服务,包括不同的靶细胞和效应细胞的筛选。下面对2个常见靶点的ADCC细胞生物学活性检测分别进行举例。
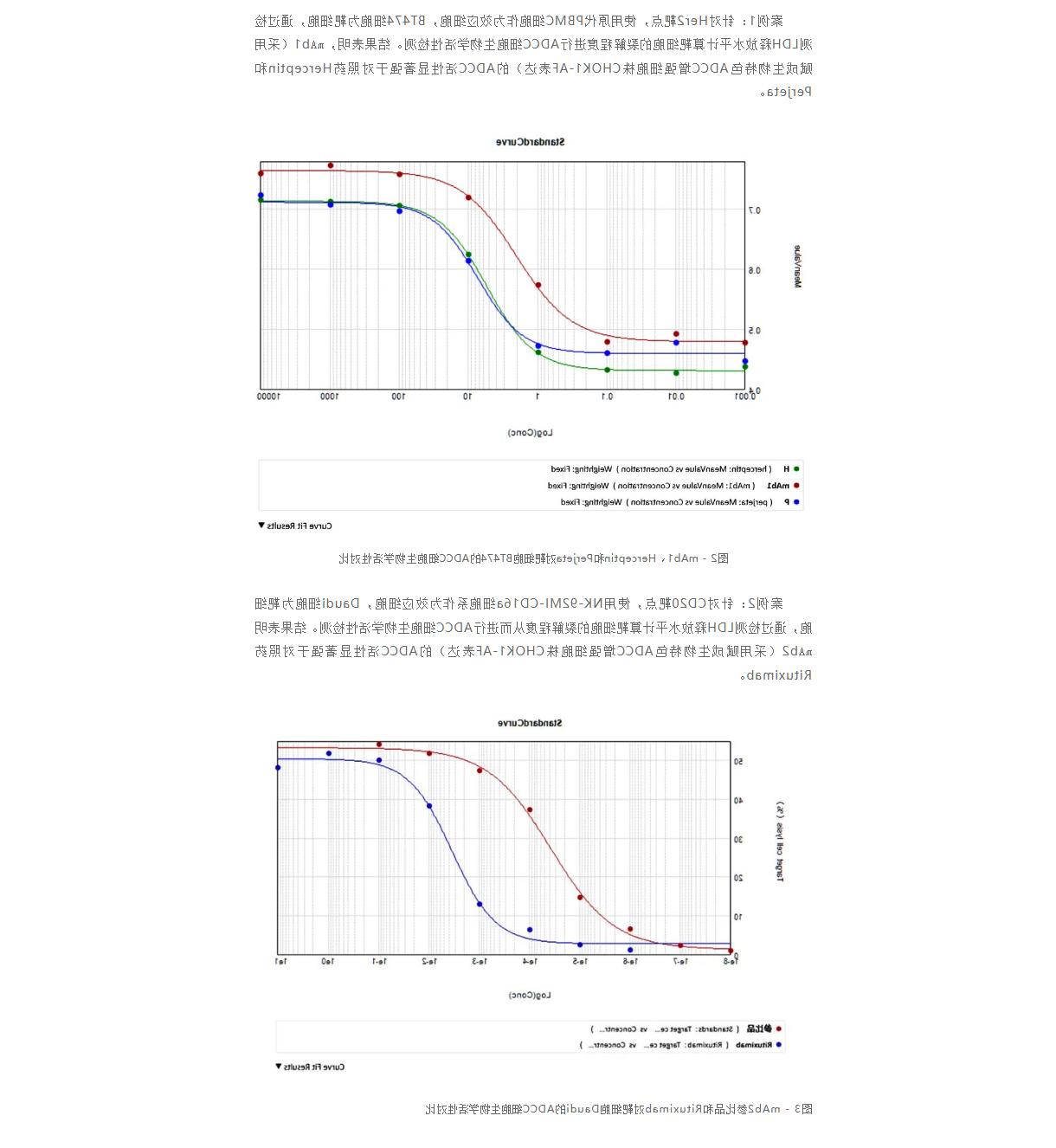
四、ADCC细胞生物学活性检测技术平台特点
团队拥有50+项目的实战经验,包括10+ ADCC增强抗体;
抗体药物常见靶点如CD20, Her2, EGFR, PD-L1, Claudin 18.2等阳性药对照经验;
热门靶点40+癌细胞系和过表达靶点细胞系(按三级细胞库管理);
NK-92MI-CD16a细胞系ADCC细胞生物学活性分析平台通过完整方法学验证;
具有丰富上市申报经验,满足新药IND和BLA申报合规性要求。
参考文献:
[1] Kubota T ,Niwa R , Satoh M , et al. Engineered therapeutic antibodies with improved effector functions[J]. Cancer Science, 2009, 100(9).
延伸阅读:







